属于卤素的一价非金属元素,正常情况下氟气是一种浅黄绿色的、有强烈助燃性的、刺激性毒气,是已知的最强的氧化剂之一,元素符号F。氟气为苍黄色气体,密度1.69克/升,熔点-219.62℃,沸点-188.14℃,化合价-1,氟的电负性最高,电离能为17.422电子伏特,是非金属中最活泼的元素,氧化能力很强,能与大多数含氢的化合物如水、氨和除氦、氖、氩外一切无论液态、固态、或气态的化学物质起反应。氟气与水的反应很复杂,主要产物是氟化氢和氧,以及较少量的过氧化氢,二氟化氧和臭氧产生,也可在化合物中置换其他非金属元素。可以同所有的非金属和金属元素起猛烈的反应,生成氟化物,并发生燃烧。有极强的腐蚀性和毒性,操作时应特别小心,切勿使它的液体或蒸气与皮肤和眼睛接触。
氟化学造价信息
元素来源:可从电解熔融的氟化钾和无水氟化氢的混合物中制得。
元素用途:液态氟可作火箭燃料的氧化剂。含氟塑料和含氟橡胶有特别优良的性能。含氟塑料和含氟橡胶等高分子,具有优良的性能,用于氟氧吹管和制造各种氟化物。
元素辅助资料:正是经过19世纪初期的化学家发反复分析,肯定了盐酸的组成,确定了氯是一种元素之后,氟就因它和氯的相似性很快被确认是一种元素,相应的存在与氢氟酸中。虽然它的单质状态一直拖延到19世纪80年代才被分离出来。氟和氯一样,也是自然界中广泛分布的元素之一,在卤素中,它在地壳中的含量仅次于氯。早在16世纪前半叶,氟的天然化合物萤石(CaF2)就被记述于欧洲矿物学家的著作中,当时这种矿石被用作熔剂,把它添加在熔炼的矿石中,以降低熔点。因此氟的拉丁名称 fluorum从fluo(流动)而来。它的元素符号由此定为F。拉瓦锡在1789年的化学元素表中将氢氟酸基当作是一种元素。到1810年戴维确定了氯气是一种元素,同一年法国科学家安培根据氢氟酸和盐酸的相似性质和相似组成,大胆推断氢氟酸中存在一种新元素。他并建议参照氯的命名给这种元素命名为fluorine。但单质状态的氟却迟迟未能制得,直到1886年6月26日,才由法国化学家弗雷米的学生莫瓦桑制得。莫瓦桑因此获得1906年诺贝尔化学奖,他是由于在化学元素发现中作出贡献而获诺贝尔化学奖的第二人。比较一下氯和氟的发现史,是很有意义的。氯在它的单质被分离出来30多年后才被确认为是一种元素;而氟在没有被分离出单质状态以前就被确认为是一种元素了。这一史实说明在人们对客观事物的认识过程中,逐渐掌握了它们的一些规律后,就能更快、更清楚地认识它们。
熔点为-219.6 ℃,沸点为-188.1 ℃,密度为1.696 g/L(0 ℃)。淡黄色气体,是最活泼的非金属元素。用于制氟化试剂以及金属冶炼中的助熔剂等。
PS:氟,原子序数9,原子量18.9984032,元素名来源于其主要矿物萤石的英文名。1812年法国科学家安培指出氢氟酸中含有一种新元素,但自由状态的氟一直没有制得。直到1886年,法国化学家穆瓦桑将氟化钾溶解在无水氢氟酸中进行电解,才制得单质氟。由于氟非常活泼,所以自然界中不存在游离状态的氟。氟在地壳中的含量为0.072%,重要的矿物有萤石、氟磷酸钙等。氟的天然同位素只有氟19。
氟是化学性质最活泼、氧化性最强的物质,,氟能同所有其他元素化合;氟与溴、碘、硫、磷、碳、硅等物质在低温下就能猛烈化合;氟离子体积小,容易与许多正离子形成稳定的配位化合物;氟与烃类会发生难以控制的快速反应,氟与NaOH反应:2NaOH+2F2=2NaF+H2O+OF2,氟与水反应:2H2O+2F2=4HF+O2。
氟是卤族中的第一个元素,但发现得最晚。从1771年瑞典化学家舍勒制得氢氟酸到1886年法国化学家莫瓦桑分离出单质氟经历了100多年时间。 在此期间,戴维、盖·吕萨克、诺克斯兄弟等很多人为制取单质氟而中毒,鲁耶特、尼克雷因中毒太深而献出了自己的生命。
莫瓦桑总结了前人的经验教训,他认为,氟活泼到无法电解的程度,电解出的氟只要一碰到一种物质就能与其化合。如果采用低温电解的方法,可能是解决问题的一个途径。经过多次实验,1886年6月26日, 法国人莫瓦桑终于在低温下用电解氟氢化钾与无水氟化氢混合物的方法制得了游离态的氟,并获诺贝尔化学奖。
氟化学简介常见问题
-
【中文名称】钠别名:氟氢化钠;二氟氢化钠;酸式氟化钠【英文名称】sodium bifluoride【CAS No.】1333-83-1【分子式】NaHF2【分子量】61.99【密度】2.08【熔点】(...
-
可溶于而生成锂。 急性毒性:LD50:200 mg/kg(豚鼠经口)。具刺激性。吸入、摄入或经皮吸收会中毒。大剂量可引起眩晕、虚脱。对有损害。 该品有毒,吸入或与皮肤接触时有毒害。对水是稍微危害的,若...
-
因为,锂离子的极化能力比钾离子强
氟化学简介文献

 浙江巨圣氟化学有限公司聚四氟乙烯工程通过竣工验收
浙江巨圣氟化学有限公司聚四氟乙烯工程通过竣工验收
浙江巨圣氟化学有限公司聚四氟乙烯工程通过竣工验收

 几种氟化碳材料的结构与电化学性能
几种氟化碳材料的结构与电化学性能
氟化碳是一种高储能密度锂原电池的正极材料,材料晶相结构对其电化学性能有重要影响。以NF3为氟化剂对多种碳源进行氟化,制备了不同层间距和比表面积系列的氟化碳材料,并进行表征和电化学测试。结果表明:通过优选碳源,可以增大氟化产物的层间距和比表面积,从而有效减小电极极化,提高电池的工作电压。
氟最重要的化合物是氟化氢。氟化氢很易溶解于水,水溶液叫氢氟酸,,这正如氯化氢的水溶液叫氢氯酸(俗名叫盐酸)一样。氢氟酸都是装在聚乙烯塑料瓶里的。如果装在玻璃瓶里的话,过一会儿,整个玻璃瓶都会被它溶解掉——因为它能强烈地腐蚀玻璃。人们便利用它的这一特性,先在玻璃上涂一层石蜡,再用刀子划破蜡层刻成花纹,涂上氢氟酸。过了一会儿,洗去残余的氢氟酸,刮掉蜡层,玻璃上便出现美丽的花纹。玻璃杯上的刻花、玻璃仪器上的刻度,都是用氢氟酸“刻”成的。由于氢氟酸会强烈腐蚀玻璃,所以在制造氢氟酸时不能使用玻璃的设备,而必须在铅制设备中进行。
在工业上,氟化氢大量被用来制造聚四氟乙烯塑料。聚四氟乙烯号称“塑料之王”,具有极好的耐腐蚀性能,即使是浸在王水中,也不会被侵蚀。它又耐250℃以上的高温和-269.3℃以下的低温。在原子能工业、半导体工业、超低温研究和宇宙火箭等尖端科学技术中,有着重要的应用。我国在1965年已试制成功“聚四氟乙烯”。聚四氟乙烯的表面非常光滑,滴水不沾。人们用它来制造自来水笔的笔尖,吸完墨水后,不必再用纸来擦净墨水,因为它表面上一点墨水也不沾。氟化氢也被用来氟化一些有机化合物。著名的冷冻剂“氟利昂”,便是氟与碳、氯的化合物。在酿酒工业上,人们用氢氟酸杀死一些对发酵有害的细菌。
氢氟酸的盐类,如氟化锶、氟化钠、氟化亚锡等,对乳酸杆菌有显著的抑制能力,被用来制造防龋牙膏。常见的“氟化锶”牙膏,便含有大约千分之一的氟化锶。
在大自然中,氟的分布很广,约占地壳总重量的万分之二。最重要的氟矿是萤石——氟化钙。萤石很漂亮,有玻璃般的光泽,正方块状,随着所含的杂质不同,有淡黄、浅绿、淡蓝、紫、黑、红等色。我国在古代便已知道萤石了,并用它制作装饰品。现在,萤石大量被用来制造氟化氢和氟。在炼铝工业上,也消耗大量的萤石,因为用电解法制铝时,加入冰晶石(较纯的氟化钙晶体)可降低氧化铝的熔点。天然的冰晶石很少,要用萤石作原料来制造。除了萤石外,磷灰石中也含有3%的氟。土壤中约平均含氟万分之二,海水中含氟约一千万分之一。
在人体中,氟主要集中在骨骼和牙齿。特别是牙齿,含氟达万分之二。牡蛎壳的含氟量约比海水含氟量高二十倍。植物体也含氟,尤其是葱和豆类含氟最多。
浙江巨圣氟化学有限公司、中蓝晨光化工研究设计院有限公司、中蓝晨光成 都检测技术有限公司
由于三氟甲基的强电负性,高稳定性和良好的脂溶性,三氟甲基的引入,往往使化合物的性质,特别是其生理活性发生显著的改变,其在新药开发中越来越被关注。所以如何将三氟甲基引入目标分子,成为氟化学中的一个重要的课题。经过多年的研究,已经发展了许多引入三氟甲基的方法,如我们前面提到的用SF4将羧基转化为三氟甲基,按照反应机理,三氟甲基的引入主要分为三大类:自由基三氟甲基化,亲核三氟甲基化和亲电三氟甲基化【Trifluoromethylations and Related Reactions in OrganicChemistry, McClinton, D. A. Tetrahedron. 1992, 48, 6555-6666.】。
一、氟代试剂之四氟化硫
二、亲核三氟甲基化反应
Prakash试剂
Burton三氟甲基化(Burton Trifluoromethylation)
Amii三氟甲基化(Amii Trifluoromethylation)
四、亲电三氟甲基化反应
六、自由基三氟甲基化
三氟甲基自由基能通过多种途径得到,由于其亲电性强,所以能与富电子的苯环发生亲电加成反应。
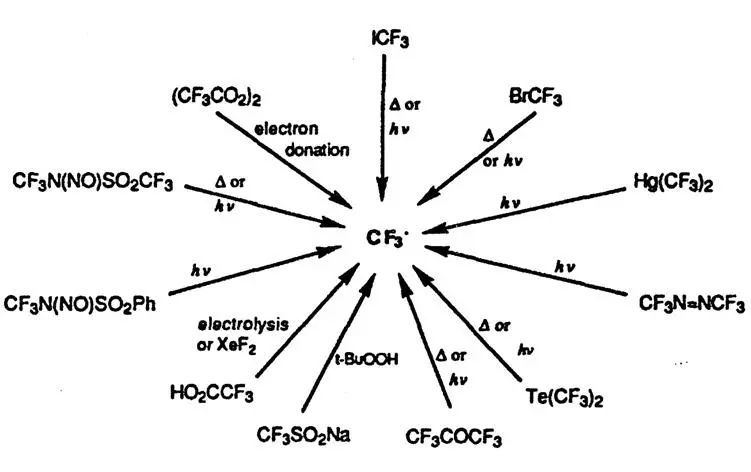
但这种方法产率低,选择性差,而且反应难于控制,所以在有机合成中的应用受到限制。
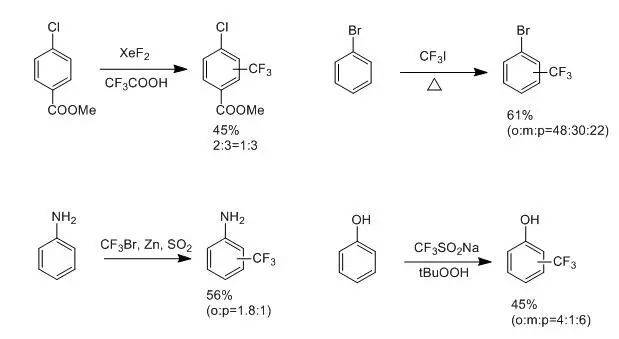
本文经本号整理汇总得到,内容非原创,如涉及版权问题请联系本号删除。
- 相关百科
- 相关知识
- 相关专栏
- 专勤消防车
- 氟化铷
- 四驱消防车
- 氟氢化钾
- 斯太尔消防车
- 氟氢酸
- 豪泺8吨消防车
- 氟化铅
- GBZ/T192.4-2007
- 轻型消防车
- 鳞片石墨粉
- 供水消防车
- 机场救援先导消防车
- 无氧酸
- 蚀刻玻璃
- 氟化镧
- 永磁同步电机简介
- 以色列ELI自清洗网式过滤器和浅层介质过滤器简介
- 有关水利水电勘测设计技术标准体系情况的简介
- 工程技术分析论文地辐射采暖系统简介及常见问题
- 工程定额及造价资料电子查阅与简易预结算编制系统简介
- 化学除油器与稀土磁盘在轧钢废水处理中应用综合分析
- 化学示踪实验技术在水利工程渗漏检测中应用(英文)
- 广(州)深(圳)准高速铁路石龙—常坪段路基施工简介
- 基于GIS技术安徽省主要防洪工程信息系统简介
- 广东省东江—深圳供水改造工程施工图设计监理工作简介
- 广州市人民政府关于加强危险化学品道路运输管理通告
- 化学灌浆技术在地下厂房岩锚梁混凝土裂缝处理中应用
- 化学灌浆技术在大花水电站大坝混凝土裂缝处理中应用
- 乐星产电乐星产电(无锡)有限公司二期工程项目简介
- 国家玻璃质量监督检验中心安全玻璃CCC认证业务简介
- 建筑工程门窗系列产品节点图及简介PPT