低温电子显微镜未来前景
洛克菲勒大学(Rockefeller University)的生物物理学家Rod MacKinnon就是这些人之一。他在2003年因解析一些离子通道的结晶结构而获得诺贝尔奖。MacKinnon现在对低温电镜非常着迷。"我现在处于学习曲线的斜坡阶段,非常热切。" MacKinnon说道。他打算用低温电镜来研究离子通道是如何开和关的。
1997年时,Henderson非常坚定地宣称,低温电镜会成为解析蛋白结构的主流工具。在将近20年后的今天,他的预测比当年有了更多底气。Henderson表示,如果低温电镜保持这样的势头继续发展,技术问题也得以解决,那么低温电镜不仅会成为解析蛋白结构的第一选择,而是主流选择。这个目标已经离我们不远了。
结构生物学家 Sjors Scheres表示,未来需要更多低温电子显微镜,未来它会成为结构生物学的主流。
低温电子显微镜造价信息
成功解析
现在低温电镜迅猛发展,专家们正在寻找更大的挑战作为下一个解析目标。对很多人来说,最想解析的是夹在细胞膜内的蛋白。这些蛋白是细胞信号通路中的关键分子,也是比较热门的药物靶标。这些蛋白很难结晶,而低温电子显微镜不大可能对单个蛋白进行成像,这是因为很难从背景噪音中提取这些信号。
加利福利亚大学(University of California)的生物物理学家程亦凡,计划解析一种细小的膜蛋白TRPV1。TRPV1是检测辣椒中引起灼烧感的物质的受体,并与其它痛感蛋白紧密相关。加利福利亚大学病理学家David Julius等人之前尝试结晶TRPV1,结果失败。
用低温电子显微镜解析TRPV1项目,一开始进展缓慢。但2013年底,技术进步使得这一项目有了重大突破,他们获得了分辨率为0.34纳米的TRPV1蛋白的结构。该成果的发表对于领域来说,无异于惊雷。因为这证实了低温电子显微镜能够解析小的、重要的分子。"当我看到TRPV1的结构时,我激动得一晚上睡不着觉。"Rubinstein说道。
研究者们可能面临更多这样无眠的夜晚。Agard表示,会有更多膜蛋白相继被解析出来。
上个月由Scheres和清华大学的结构生物学家施一公合作用低温电子显微镜成功解析了一个膜蛋白。他们建立了γ-分泌酶的模型,γ-分泌酶负责合成与阿兹海默症相关的β-淀粉斑。0.34纳米分辨率的图谱显示,比较少见的遗传性阿尔茨海默病的γ-分泌酶突变后会在图谱上呈现两个"热点"(突变或者重组频率显着增加的位点),并且这种突变最终会合成有毒性的β-淀粉斑。γ-分泌酶的结构图帮助研究者发现为什么以往的抑制剂会无效,从而促进新药的研发。程亦凡表示,γ-分泌酶的结构非常惊人。
类似的成功吸引了制药公司的注意。他们希望借助低温电子显微镜去解析那些无法结晶的蛋白,从而更好地研发药物。Scheres如今和辉瑞公司合作,攻克离子通道。离子通道包含很多膜蛋白,例如痛感受分子和神经递质受体。"我几乎被每一个人联系过。"Nogales说道。
提高性能
尽管低温电子显微镜发展迅速,很多研究者认为,它仍有巨大提升空间。他们希望能制造出更灵敏的电子探测器,以及更好地制备蛋白样本的方法。这样的话,就能够对更小的、更动态的分子进行成像,并且分辨率更高。5月,有研究者发表了一篇细菌蛋白的结构,分辨率达到了0.22纳米。这也显示了低温显微镜的潜力。
面对问题
与任何热门领域一样,低温电子显微镜的发展也有烦恼。一些专家担心研究者们盲目追求该仪器会诱发一些问题。2013年HIV表面蛋白的结构图遭到了科学家们的质疑,他们认为用于建模的图片很多都是白噪声。此后,其他团队得到的X射线晶体衍射和低温电子显微镜模型也对原模型提出了质疑。但这些研究者们坚持相信自己的结果。2015年6月,在高登研究会议(Gordon Research Conference )上,研究者们希望低温电子显微镜的结构图要有严格的质量控制。并且杂志要求作者们提供详细的建模方法。
成本问题可能会限制低温电子显微镜的推广。Scheres估计,LMB每天用于支持低温电子显微镜的经费就达到近3万人民币,外加近1万的电费--这是由于存储和处理图片的电脑耗电量很大。Scheres表示,每天至少要花费近4万人民币,对于很多地方来说,这个费用太高。为了推广低温电子显微镜,很多基金会建立了对外公开的设备,各地研究者们可以预约使用。霍华德·休斯医学研究所(Howard Hughes Medical Institute, HHMI)在珍利亚农场研究园区配备了一台。这台设备对所有HHMI资金的研究者公开。在英国,政府和维康信托在牛津大学附近建立了低温电镜公开使用平台。参与该平台搭建的伦敦大学(University of London)的结构生物学家Helen Saibil表示,有很多人想学习使用低温电镜。
X射线晶体衍射一直是结构生物学家的最佳工具,但是它有较大的限制。科学家们可能需要几年才能找到把蛋白形成大块结晶的方法。而很多基础蛋白分子,例如嵌在细胞膜上的蛋白,或是形成复合体的蛋白却无法被结晶。
20世纪80年代和90年代,低温电子显微镜领域发展迅速。一个关键性突破是利用液态乙烷来快速冷冻蛋白溶液。这也是为什么叫低温电子显微镜的原因。这个技术的分辨率仅为1纳米,远远达不到针对蛋白结构进行药物设计的需求。而当时X射线晶体衍射的分辨率能达到0.4纳米。NIH等资助者投入了数亿美金来支持蛋白晶体领域的发展,但对于低温电子显微镜领域的资助却很少。
1997年,Henderson参加了高登研究会议(Gordon Research Conference )关于3D电子显微镜的年会。一位同事以这样的话做为开幕致词,"低温电子显微镜技术非常有限,不可能超越X射线晶体衍射。" 但Henderson的想法完全不同,在下一场发言中,他做出了反击。Henderson指出,低温电子显微镜会超越其它各种技术,成为全球研究蛋白结构的主流工具。
低温电子显微镜未来前景常见问题
-
电子显微镜的分类 1、透射电镜 (TEM) 样品必须制成电子能穿透的,厚度为100~2000 Å的薄膜。成像方式与光学生物显微镜相似,只是以电子透镜代替玻璃透镜。放大后的电子像在荧光屏上显示出来,TE...
-
电子显微镜是根据电子光学原理,用电子束和电子透镜代替光束和光学透镜,使物质的细微结构在非常高的放大倍数下成像的仪器。 电子显微镜的分辨能力以它所能分辨的相邻两点的最小间距来表示。20世纪70年代,透射...
-
顾名思义,所谓电子显微镜是以电子束为照明光源的显微镜。由于电子束在外部磁场或电场的作用下可以发生弯曲,形成类似于可见光通过玻璃时的折射现象,所以我们就可以利用这一物理效应制造出电子束的“透镜”,从而开...
低温电子显微镜震惊了结构生物学。过去30年里,低温电子显微镜揭示了核糖体、膜蛋白和其它关键细胞蛋白的精细结构。这些发现都发表在顶级杂志上。结构生物学家们表示,毫不夸张地说,低温电子显微技术正处于革命之中:低温电子显微镜能够快速生成高分辨率的分子模型,这一点远超X射线晶体衍射等方法。依靠旧方法获得诺奖的实验室也在努力学习这一技术。这种新模型能够准确地揭示细胞运行的必要机制,以及如何靶向针对疾病相关的蛋白。
"低温电子显微镜能够解决很多以前无法解决的谜题。"旧金山加利福利亚大学(University of California)的结构生物学家David Agard这样说道。
几年前Scheres被招进LMB,任务是帮助改进低温电子显微镜,最终他成功了。上个月,他们发表了这个领域最令人振奋的成就:阿兹海默症相关的酶的高清图片,图片包括该酶的1200左右个氨基酸,分辨率达到零点几纳米。
生物学家们如今仍在努力发展该技术,以期用它解决小分子或可变形分子的精微结构--这对低温电子显微镜来说,也是一大挑战。来自加利福利亚大学的结构生物学家Eva Nogales表示,低温电子显微镜打开了一扇大门。
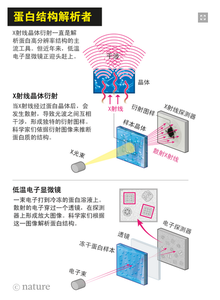
低温电子显微镜生物仪器
低温电子显微镜,通过电子束对冷冻的生物分子进行成像,从而得到分子的三维结构。
目前,低温电子显微镜非常敏感,一声喊叫就会带来极大误差,导致实验失败。
世界上最先进的低温电子显微镜之一:位于英国医学研究委员会分子生物学实验室(UK Medical Research Council Laboratory of Molecular Biology, LMB),770万美金,外形笨重,是个大约3米高的金属盒子通过连接细胞的橙色缆线,可以传输以万亿字节计算的数据。
2013年末,《Nature Methods》杂志将年度技术授予了单细胞测序(single-cell sequencing)。同时,杂志还介绍了2014年值得关注的技术,其中就包括单粒子低温电子显微镜。
2013年发表的两篇文章介绍了美国加州大学旧金山分校的研究人员利用一种新开发的单电子计数探测器,证实了电子束诱导的移动会大幅降低分辨率,并且,他们发现,快速读取与几乎无噪音的电子计数的组合使图像模糊得以校正,将图像信息恢复到高分辨率。
2015年结构生物学出现里程碑式进展,低温电子显微镜技术时代来临。
低温电子显微镜震惊了结构生物学。过去30年里,低温电子显微镜揭示了核糖体、膜蛋白和其它关键细胞蛋白的精细结构。这些发现都发表在顶级杂志上。结构生物学家们表示,毫不夸张地说,低温电子显微技术正处于革命之中:低温电子显微镜能够快速生成高分辨率的分子模型,这一点远超X射线晶体衍射等方法。依靠旧方法获得诺奖的实验室也在努力学习这一技术。这种新模型能够准确地揭示细胞运行的必要机制,以及如何靶向针对疾病相关的蛋白。
"低温电子显微镜能够解决很多以前无法解决的谜题。"旧金山加利福利亚大学(University of California)的结构生物学家David Agard这样说道。
Scheres被招进LMB时,任务是帮助改进低温电子显微镜,最终他成功了。2015年8月,他们发表了这个领域最令人振奋的成就:阿兹海默症相关的酶的高清图片,图片包括该酶的1200左右个氨基酸,分辨率达到零点几纳米。
生物学家们如今仍在努力发展该技术,以期用它解决小分子或可变形分子的精微结构--这对低温电子显微镜来说,也是一大挑战。来自加利福利亚大学(University of California)的结构生物学家Eva Nogales表示,叫它革命也好,飞跃也好,低温电子显微镜的确打开了一扇大门。
低温电子显微镜未来前景文献

 原子水平的表面特征传感器—扫描式隧道电子显微镜(STM)
原子水平的表面特征传感器—扫描式隧道电子显微镜(STM)
原子水平的表面特征传感器—扫描式隧道电子显微镜(STM)

 扫描电子显微镜在PS版铝板基砂目形貌观察中的应用
扫描电子显微镜在PS版铝板基砂目形貌观察中的应用
用扫描电子显微镜(SEM)对PS版铝板基上的砂目形貌进行了观察分析,比较了不同砂目形貌对PS版性能的影响。实践证明,SEM可以方便直观地观察铝板基上砂目的细密程度、平台和深度,为砂目的处理提供客观可靠的依据。

电子显微镜种类
电子显微镜按结构和用途可分为透射式电子显微镜、扫描式电子显微镜、反射式电子显微镜和发射式电子显微镜等。
透射式电子显微镜常用于观察那些用普通显微镜所不能分辨的细微物质结构;扫描式电子显微镜主要用于观察固体表面的形貌,也能与X射线衍射仪或电子能谱仪相结合,构成电子微探针,用于物质成分分析;发射式电子显微镜用于自发射电子表面的研究。
电子显微镜透射电子显微镜
因电子束穿透样品后,再用电子透镜成像放大而得名。它的光路与光学显微镜相仿,可以直接获得一个样本的投影。通过改变物镜的透镜系统人们可以直接放大物镜的焦点的像。由此人们可以获得电子衍射像。使用这个像可以分析样本的晶体结构。在这种电子显微镜中,图像细节的对比度是由样品的原子对电子束的散射形成的。由于电子需要穿过样本,因此样本必须非常薄。组成样本的原子的原子量、加速电子的电压和所希望获得的分辨率决定样本的厚度。样本的厚度可以从数纳米到数微米不等。原子量越高、电压越低,样本就必须越薄。样品较薄或密度较低的部分,电子束散射较少,这样就有较多的电子通过物镜光栏,参与成像,在图像中显得较亮。反之,样品中较厚或较密的部分,在图像中则显得较暗。如果样品太厚或过密,则像的对比度就会恶化,甚至会因吸收电子束的能量而被损伤或破坏。
透射电镜的分辨率为0.1~0.2nm,放大倍数为几万~几十万倍。由于电子易散射或被物体吸收,故穿透力低,必须制备更薄的超薄切片(通常为50~100nm)。
透射式电子显微镜镜筒的顶部是电子枪,电子由钨丝热阴极发射出、通过第一,第二两个聚光镜使电子束聚焦。电子束通过样品后由物镜成像于中间镜上,再通过中间镜和投影镜逐级放大,成像于荧光屏或照相干版上。中间镜主要通过对励磁电流的调节,放大倍数可从几十倍连续地变化到几十万倍;改变中间镜的焦距,即可在同一样品的微小部位上得到电子显微像和电子衍射图像。
电子显微镜扫描电子显微镜
扫描电子显微镜的电子束不穿过样品,仅以电子束尽量聚焦在样本的一小块地方,然后一行一行地扫描样本。入射的电子导致样本表面被激发出次级电子。显微镜观察的是这些每个点散射出来的电子,放在样品旁的闪烁晶体接收这些次级电子,通过放大后调制显像管的电子束强度,从而改变显像管荧光屏上的亮度。图像为立体形象,反映了标本的表面结构。显像管的偏转线圈与样品表面上的电子束保持同步扫描,这样显像管的荧光屏就显示出样品表面的形貌图像,这与工业电视机的工作原理相类似。由于这样的显微镜中电子不必透射样本,因此其电子加速的电压不必非常高。
扫描式电子显微镜的分辨率主要决定于样品表面上电子束的直径。放大倍数是显像管上扫描幅度与样品上扫描幅度之比,可从几十倍连续地变化到几十万倍。扫描式电子显微镜不需要很薄的样品;图像有很强的立体感;能利用电子束与物质相互作用而产生的次级电子、吸收电子和X射线等信息分析物质成分。
扫描电子显微镜的制造是依据电子与物质的相互作用。当一束高能的入射电子轰击物质表面时,被激发的区域将产生二次电子、俄歇电子、特征x射线和连续谱X射线、背散射电子、透射电子,以及在可见、紫外、红外光区域产生的电磁辐射。同时,也可产生电子-空穴对、晶格振动(声子)、电子振荡(等离子体)。
电子显微镜发展历史
1926年汉斯·布什研制了第一个磁力电子透镜。
1931年厄恩斯特·卢斯卡和马克斯·克诺尔研制了第一台透视电子显微镜。展示这台显微镜时使用的还不是透视的样本,而是一个金属格。1986年卢斯卡为此获得诺贝尔物理奖。
1934年锇酸被提议用来加强图像的对比度。
1937年第一台扫描透射电子显微镜推出。一开始研制电子显微镜最主要的目的是显示在光学显微镜中无法分辨的病原体如病毒等。
1938年他在西门子公司研制了第一台商业电子显微镜。
1949年可透射的金属薄片出现后材料学对电子显微镜的兴趣大增。
1960年代透射电子显微镜的加速电压越来越高来透视越来越厚的物质。这个时期电子显微镜达到了可以分辨原子的能力。
1980年代人们能够使用扫描电子显微镜观察湿样本。
1990年代中电脑越来越多地用来分析电子显微镜的图像,同时使用电脑也可以控制越来越复杂的透镜系统,同时电子显微镜的操作越来越简单。
电子显微镜参数
电子显微镜分辨率
分辨能力是电子显微镜的重要指标,电子显微镜的分辨能力以它所能分辨的相邻两点的最小间距来表示,即称为该仪器的最高点分辨率:d=δ。显然,分辨率越高,即d的数值(为长度单位)愈小,则仪器所能分清被观察物体的细节也就愈多愈丰富,也就是说这台仪器的分辨能力或分辨本领越强。
分辨率与透过样品的电子束入射锥角和波长有关。可见光的波长约为300~700纳米,而电子束的波长与加速电压有关。依据波粒二象性原理,高速的电子的波长比可见光的波长短,而显微镜的分辨率受其使用的波长的限制,因此电子显微镜的分辨率(0.2纳米)远高于光学显微镜的分辨率(200纳米)。当加速电压为50~100千伏时,电子束波长约为0.0053~0.0037纳米。由于电子束的波长远远小于可见光的波长,所以即使电子束的锥角仅为光学显微镜的1%,电子显微镜的分辨本领仍远远优于光学显微镜。光学显微镜的最大放大倍率约为2000倍,而现代电子显微镜最大放大倍率超过300万倍,所以通过电子显微镜就能直接观察到某些重金属的原子和晶体中排列整齐的原子点阵。
电子显微镜放大率
单就放大率(magnification)而言,是指被观察物体经电子显微镜放大后,在同一方向上像的长度与物体实际长度的比值。这是两条直线的比值,有人将放大率理解为像与物的面积比,这是一种误解,势必引起概念上的混淆和计算方法与结果上的混乱。
以下列举电镜常见的应用(截至1984年),其在对外贸易和军事等其他领域也有其用武之地 。
电子显微镜物理学
分子和原子形态的研究;晶体薄膜位错和层错的研究;表面物理现象的研究等 。
电子显微镜化学
高分子结构和性能方面的研究;一些有机复合材料的结构形态和添加剂的研究;催化剂的研究:各种无机物质性能、结构、杂质含盘的研究;甚至对一些化学反应过程的研究等 。
电子显微镜生物学
在分子生物学、分子遗传学及遗传工程方面的研究;昆虫分类的研究:人工合成蛋白质方面的研究以及对各种细菌;病毒、噬菌体等微生物的研究 。
电子显微镜医药卫生
癌症发病机理的研究及早期诊断;药理及病理学方面的研究;计划生育和节育药物的研究;对病毒及干扰素方面的研究以及临床诊断等 。
电子显微镜技术在肿瘤诊断中的应用
因此,透射电子显微镜突破了光学显微镜分辨率低的限制,成为了诊断疑难肿瘤的一种新的工具。有研究报道,无色素性肿瘤、嗜酸细胞瘤、肌原性肿瘤、软组织腺泡状肉瘤及神经内分泌肿瘤这些在光镜很难明确诊断的肿瘤,利用电镜可以明确诊断电镜主要是通过对超微结构的精细观察,寻找组织细胞的分化标记,确诊和鉴别相应的肿瘤类型。细胞凋亡与肿瘤有着密切的关系,电镜对细胞凋亡的研究起着重要的作用,因此利用电镜观察细胞的超微结构病理变化和细胞凋亡情况,将为肿瘤的诊断和治疗提供科学依据。
电子显微镜技术在肿瘤鉴别诊断中的应用
透射电子显微镜观察的是组织细胞、生物大分子、病毒、细菌等结构,能够观察到不同病的病理结构,也可以鉴别一些肿瘤疾病,有研究报道电子显微镜技术通过超微结构观察可以区分癌、黑色素瘤和肉瘤以及腺癌和间皮瘤;可区别胸腺瘤、胸腺类癌、恶性淋巴瘤和生殖细胞瘤;可区别神经母细胞瘤、胚胎性横纹肌瘤、Ewing氏肉瘤、恶性淋巴瘤和小细胞癌;可区别纤维肉瘤、恶性纤维组织细胞瘤、平滑肌肉瘤和恶性神经鞘瘤以及区别梭形细胞癌和癌肉瘤。
电子显微镜地质与考古
地层的研究、分析、识别:矿石的分析研究:化石、古尸、古瓷及各种出土文物的分析研究:文物古董的真伪鉴别等 。
电子显微镜冶金
精密合金的性能和工艺研究;钢铁材料断口分析和夹杂物成分及分布的分析研究;耐高温、高强度金属材料及超导材料等的研究;金相分析等 。
电子显微镜电子元件
各种半导体器件如超大规模集成电路等的失效分析和性能检查;硅单晶等各种半导体材料性能的分析研究;各种开关、电位器.接插件的可靠性研究及耐久性分析;录音磁带.磁粉晶形的分析检查等 。
电子显微镜机械工业
热处理工艺、焊接工艺、铸造工艺等等的研究;破损机件的断口分析等 。
电子显微镜石油化工
油田岩芯的研究分析:石油制品性能结构的研究和成分分析;催化剂的研究等等 。
电子显微镜纺织、轻工业
羊毛纤维、纸张和粮食等的质量评定;畲成纤维性能的研究:感光胶片的乳剂的研究等等 。
电子显微镜硅酸盐及无机材料
各种陶瓷、玻璃、云母、石墨、人造金刚石及新型建筑材料的性能结构和工艺研究和成分分析 。
电子显微镜原子能
放射性同位素以及反应堆所用特殊材料的研究分析 。
电子显微镜航空和空间技术
航空和宇航特种材料的研究:高空生理和太空生理的研究;宇宙物质的研究分析等 。
电子显微镜农林、畜牧
由于植物病毒引起的粮食、果树、烟草等作物的病害的防治研究;家畜、家禽、战马等发生癌病的动物病毒的研究;杂交优势以及诱发突变的研究 。
电子显微镜法学
刑事案件中对尸体、假币、锁钥。凶器及各种作案工具的判别与分析,为破案提供充分的证据 。
电子显微镜环境保护
大气或水中的固体粉尘、微粒的分析研究和粒度测定等 。
- 相关百科
- 相关知识
- 相关专栏
- 电子显微镜技术与应用
- 每井泉净水器
- 场发射环境扫描电子显微镜
- 奥林巴斯显微镜SZX7
- LEICAMZ9s体视显微镜
- YZ5G裂隙灯显微镜
- 水力清
- 倒置荧光显微镜
- 3MAP801
- Leica倒置荧光显微镜
- 逆渗透技术
- 电子扫描显微镜
- 多光子激光扫描显微镜
- 暗场显微镜
- 干涉显微镜
- 杀菌热水器
- 中国吹制玻璃行业市场前景分析预测年度报告(目录)
- 中国电力井盖行业市场前景分析预测年度报告(目录)
- 中国轨道射灯行业市场前景分析预测年度报告
- 中国仿古青砖行业市场前景分析预测年度报告(目录)
- 中国家具钢管行业市场前景分析预测年度报告(目录)
- 中国读卡器市场现状分析及未来五年发展前景分析报告
- 中国水泥沟盖板市场发展及投资前景报告
- 中国亚克力板行业市场前景分析预测年度报告(目录)
- 制水泥楼板市场现状调研及发展前景分析报告(目录)
- 中国运用现代集成制造技术改造传统产业的经验和前景
- 中国碳工钢产业深度调研及未来五年发展定位分析报告
- 中国大理石石材市场发展及投资前景报告
- 中国钢丝切丸行业市场前景分析预测年度报告(目录)
- 中国钢结构承包市场调查及未来五年投资前景评估报告
- 中国移动板房行业市场前景分析预测年度报告(目录)
- 中国手工地毯行业市场前景分析预测年度报告
