电极电位
电极电位基本信息
| 中文名 | 电极电位 | 性 质 | 科学 |
|---|---|---|---|
| 类 别 | 化学 | 解 释 | 金属的表面与溶液间产生电位差 |
判断氧化还原反应自发进行的方向
电池反应都是自发进行的氧化还原反应。因此电池反应的方向即氧化还原反应自发进行的方向。判断氧化还原反应进行的方向时,可将反应拆为两个半反应,求出电极电位。然后根据电位高的为正极起还原反应,电位低的为负极起氧化反应的原则,就可以确定反应自发进行的方向。如果两个电对的值相差较大(即Eφ),浓度的变化对电位的影响不大,不至于使反应改变方向。因此,当Eφ>0.2V 时,即使不处于标准状态,也可直接用 值的大小确定反应方向。否则,必须考虑浓度和酸度的影响,用能斯特方程式计算出电对的值,用E>0作为判断确定反应进行的方向,若E>0,正向反应能自发进行;E<0,正向反应不能自发进行,其逆向反应能自发进行。
例9 判断298K时下列反应进行的方向:
Cu2+ +2Fe2+=Cu+2Fe3+
解:将上述反应写成两个半反应,并查出它们的标准电极是位:
Cu2+ + 2e- → Cu (1)
Fe2+ - 2e- → Fe3+ (2)
标准电动势为:Eφ=2-1=0.3402-(-0.4402)
=0.7804(V)。
因为Eφ>0.2V,可直接用值判断反应进行的方向。2>1,表明Cu2+是比Fe2+更强的氧化剂,Fe是比Cu更强的还原剂所以上述反应可自发地向右进行。
为了证明这个结论的正确性,我们可以按非标准态的电池反应计算电动势。
电池电动势为:E=2-1=0.1923-(-0.4402)
=0.6325(V)
因为E>0,上述反应可自发地向右进行。
例10 判断298K时反应
当[HAsO2]=[H3AsO4]=1mol.L-1,[I-]=1mol.L-1,在中性和酸性([H+]=1mol.L-1)溶液中反应进行的方向。
解:将上述反应写成两个半反应,并查出它们的标准电极电位:
在中性溶液中,[H+]=1.0*10-71mol.L-1。
1=1=+0.535V
=0.559+0.059161g[H+]
=0.559+0.059161g10-7
=0.559+0.414
=0.145(V)
因为 12,所以I2是比H3AsO4更强的氧化剂,而HAsO2是比I-更强的还原
剂。因而上述反应能自发地向右进行。即
HAsO2+I2+2H2O→H3AsO4+2I-+2H+
当溶液中氢离子浓度为1mol.L-1时,
1=1=+0.535V
2=2=+0.559V
因为1< 2,所以H3AsO4是比I2更强的氧化剂,而I-更强的还原剂。因而上
述反应能自发地向右进行。即
H3AsO4+2I-+2H+→HAsO2+I2+2H2O
判断氧化还原反应进行的程度
氧化还原反应属可逆反应,同其他可逆反应一样,在一定条件下也能达到平衡。随着反应不断进行,参与反应的各物质浓度不断改变,其相应的电极电位也在不断变化。电极电位高的电对的电极电位逐渐降低,电极电位低的电对的电极电位逐渐升高。最后必定达到两电极电位相等,则原电池的电动势为零,此时反应达到了平衡,即达到了反应进行的限度。利用能斯特方程式和标准电极电位表可以算出平衡常数,判断氧化还原反应进行的程度。若平衡常数值很小,表示正向反应趋势很小,正向反应进行得不完全;若平衡常数值很大,表示正向反应可以充分地进行,甚至可以进行到接近完全。因此平衡常数是判断反应进行 程度的标志。
氧化还原K与反应中两个电对的标准电极电位的关系为:
(6-4)
式中,n—反应中得失电子数;
1—正反应中作为氧化剂的电对的标准电极电位;
2—正反应中作为还原剂的电对的标准电极电位。
由式(6-4)可见,1与2之差值愈大,K值也愈大,反应进行得也愈完全。
例11 计算下列反应在298K时的平衡常数,并判断此的以应进行的程度。
解: 电极反应Ag++e-→Ag 1=+0.7996V
Fe2+→Fe3++e-2=+0.77V
此反应平衡常数很小,表明此正反应进行得很不完全。
例12 计算下列反应的298K时的平衡常数,并判断此反应进行的程度。
电极电位造价信息
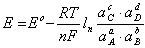
电极电位基本关系
金属可以看成是由离子和自由电子组成。
金属离子以点陈排列,电子在其间运动。对于给定的电极而言,电极电位是一个确定的常量,对于下述电极反应:
aA+bB<=>cC+dD+ne
电极电位可表示为
(1.1)
式中
E:电极电位,V;
Eo:标准电极电位,V;
R:气体常数,8.31441J/(mol·k);
T:绝对温度,k;
n:参与电极反应的电子数;
F:法拉第常数,96486.7C/mol;
a:参与化学反应各物质的活度。
式(1.1)是电极电位的基本关系式。
单个的电极电位是无法测量的,因为当用导线连接溶液时,又产生了新的溶液-电极界面,形成了新的电极,这时测得的电极电位实际上已不再是单个电极的电位,而是两个电极的电位差了。同时,只有将欲研究的电极与另一个作为电位参比标准的电极电位组成原电池,通过测量该原电池的电动势,才能确定所研究的电极的电位。
标准电极电位是以标准氢原子作为参比电极,即氢的标准电极电位值定为0,与氢标准电极比较,电位较高的为正,电位较低者为负。如氢的标准电极电位H2←→H 为0.000V,锌标准电极电位Zn ←→Zn2 为-0.762V,铜的标准电极电位Cu ←→Cu2 为 0.337V。
金属浸在只含有该金属盐的电解溶液中,达到平衡时所具有的电极电位,叫做该金属的平衡电极电位。当温度为25℃,金属离子的有效浓度为1mol/L(即活度为1)时测得的平衡电位,叫做标准电极电位。
电极电位常见问题
-
楼上回答的都不对。氢电极只是标准电极,我们人为的把它的电位定为“0”,以此来比较出其它电极电位的大小。电化学科研中,常用的参比电极是甘汞电极,因为它的制备比较容易(简单)。25摄氏度下c的电极电位数据...
-
Hg 0.242 和 Ag 0.199
-
电子或电器装置、设备中的一种部件,用做导电介质(固体、气体、真空或电解质溶液)中输入或导出电流的两个端。输入电流的一极叫阳极或正极,放出电流的一极叫阴极或负极。电极有各种类型,如阴极、阳极、焊接电极、...
判断氧化还原反应自发进行的方向
电池反应都是自发进行的氧化还原反应。因此电池反应的方向即氧化还原反应自发进行的方向。判断氧化还原反应进行的方向时,可将反应拆为两个半反应,求出电极电位。然后根据电位高的为正极起还原反应,电位低的为负极起氧化反应的原则,就可以确定反应自发进行的方向。如果两个电对的值相差较大(即Eθ),浓度的变化对电位的影响不大,不至于使反应改变方向。因此,当Eθ>0.2V 时,即使不处于标准状态,也可直接用 值的大小确定反应方向。否则,必须考虑浓度和酸度的影响,用能斯特方程式计算出电对的值,用E>0作为判断确定反应进行的方向,若E>0,正向反应能自发进行;E<0,正向反应不能自发进行,其逆向反应能自发进行。
例1 判断298K时下列反应进行的方向:
Cu2 (0.00001mol·L-1) Fe ≒ Cu Fe2 (1.0mol·L)
解:将上述反应写成两个半反应,并查出它们的标准电极电位:
Cu2 2e- → Cu
Fe2 2e- → Fe
标准电动势为:
因为
为了证明这个结论的正确性,我们可以按非标准态的电池反应计算电动势。
E1=
=0.340V
=0.340V - 0.148V
=0.192V
E2=
E=E1-E2=0.192V - (-0.44V) = 0.632V
因为E>0,上述反应可自发地向右进行。
例2 判断298K时反应
当[HAsO2]=[H3AsO4]=1mol·L-1,[I-]=1mol·L-1,在中性和酸性([H ]=1mol·L-1)溶液中反应进行的方向。
解:将上述反应写成两个半反应,并查出它们的标准电极电位:
I2 2e- ≒ 2I-
H3AsO4 2H 2e- ≒ HAsO2 2H2O
在中性溶液中,[H ]=1.0×10-7mol·L-1,
E1=
E2=
=0.560V 0.0592Vlg10-7
=0.560V-0.414V
=0.146(V)
因为E1 >E2,所以I2是比H3AsO4更强的氧化剂,而HAsO2是比I-更强的还原剂。因而上述反应能自发地向右进行。即:
HAsO2 I2 2H2O → H3AsO4 2I- 2H
当溶液中氢离子浓度为1mol·L-1时,
E1=
E2=
因为E1
H 3AsO 4 2I - 2H →HAsO 2 I 2 2H 2O
判断氧化还原反应进行的程度
氧化还原反应属可逆反应,同其他可逆反应一样,在一定条件下也能达到平衡。随着反应不断进行,参与反应的各物质浓度不断改变,其相应的电极电位也在不断变化。电极电位高的电对的电极电位逐渐降低,电极电位低的电对的电极电位逐渐升高。最后必定达到两电极电位相等,则原电池的电动势为零,此时反应达到了平衡,即达到了反应进行的限度。利用能斯特方程式和标准电极电位表可以算出平衡常数,判断氧化还原反应进行的程度。若平衡常数值很小,表示正向反应趋势很小,正向反应进行得不完全;若平衡常数值很大,表示正向反应可以充分地进行,甚至可以进行到接近完全。因此平衡常数是判断反应进行 程度的标志。
氧化还原K θ与反应中两个电对的标准电极电位的关系为:
lgkθ=
式中, n—反应中得失电子数;
由式(1-1)可见,
例3 计算下列反应在298K时的平衡常数,并判断此的以应进行的程度。
Ag Fe 2 ≒ Ag Fe 3
解: 将上述反应写成两个半反应,并查出它们的标准电极电位:
Ag
e
- ≒ Ag
Fe
3 e
- ≒ Fe
2
lgk
θ =
K θ=2.983
此反应平衡常数很小,表明此正反应进行得很不完全。
电极电位物理关系式
金属可以看成是由离子和自由电子组成。
金属离子以点陈排列,电子在其间运动。对于给定的电极而言,电极电位是一个确定的常量,对于下述电极反应:
aA bB<=>cC dD ne
电极电位可表示为
(1.1)
式中
E:电极电位,V;
Eo:标准电极电位,V;
R:气体常数,8.31441J/(mol·k);
T:绝对温度,k;
n:参与电极反应的电子数;
F:法拉第常数,96486.7C/mol;
a:参与化学反应各物质的活度。
式(1.1)是电极电位的基本关系式。
单个的电极电位是无法测量的,因为当用导线连接溶液时,又产生了新的溶液-电极界面,形成了新的电极,这时测得的电极电位实际上已不再是单个电极的电位,而是两个电极的电位差了。同时,只有将欲研究的电极与另一个作为电位参比标准的电极电位组成原电池,通过测量该原电池的电动势,才能确定所研究的电极的电位。
电极电位文献

 水位电极,超高纯水位电极,锅炉水位电极,电极式水位传感器
水位电极,超高纯水位电极,锅炉水位电极,电极式水位传感器
水位电极 一、水位电极的概述 Co-fly 系列电接点水位计,主要用于锅炉汽包、高低加热器、除氧器、蒸发器、直流锅炉起动分离器、水箱 等的水位测量。本装置由测量筒和二次仪表组成。采用数码显示和汽红水绿双色发光二极管显示液位。 二、仪表的特点及技术参数 1.水位电极的特点: ①具有闪光、声音报警功能。 ②具有 4-20mA 信号输出,可接 DCS 系统,设有保护联锁输出功能。 ③具有自供电功能,断电后可继续工作 4 小时。 ④仪表上设有三个按钮, a报警消音、 b排污按钮、 c检测按钮。 2.水位电极的技术参数: ①电源电压: 220V±10% 、50Hz ②工作环境温度: -10-45℃ ③工作相对湿度:≤ 85% ④液体水阻范围: 0-500KΩ ⑤继电器输出接点容量: 220V、3A ⑥水位显示点数: 5-19点 (最多可达 38点 ) 例如 19点: 0、± 15、± 30、± 50

 pH玻璃电极膜电位的形成及其应用
pH玻璃电极膜电位的形成及其应用
pH玻璃电极对溶液中H+的选择性响应,关键在于其敏感膜中膜电位的形成。因此准确理解膜电位形成的思维逻辑非常必要,该思维逻辑就是模型思维与函数思维的联合运用。鉴于此,本文阐述了膜电位形成所采纳的模型及其计算公式推导,并对pH玻璃电极发展趋势进行了讨论。
标准电极电位是以标准氢原子作为参比电极,即氢的标准电极电位值定为0,与氢标准电极比较,电位较高的为正,电位较低者为负。如氢的标准电极电位H2←→H 为0.000V,锌标准电极电位Zn ←→Zn2 为-0.762V,铜的标准电极电位Cu ←→Cu2 为 0.337V。
金属浸在只含有该金属盐的电解溶液中,达到平衡时所具有的电极电位,叫做该金属的平衡电极电位。当温度为25℃,金属离子的有效浓度为1mol/L(即活度为1)时测得的平衡电位,叫做标准电极电位 。
单个的电极电位是无法测量的,因为当用导线连接溶液时,又产生了新的溶液-电极界面,形成了新的电极,这时测得的电极电位实际上已不再是单个电极的电位,而是两个电极的电位差了。同时,只有将欲研究的电极与另一个作为电位参比标准的电极电位组成原电池,通过测量该原电池的电动势,才能确定所研究的电极的电位 。2100433B
一、使用说明
二、络合剂的略语符号
三、各元素的标准电极电位数据表
- 相关百科
- 相关知识
- 相关专栏
- 拾级而下
- 益阳市资阳区鑫诚园林
- 差动保护
- 嘉俊园林
- 差分信号
- 2-吡嗪-2-基乙醇
- N,N-二乙醇十二酰胺
- 消防安全知识
- 山毛桃
- 电流
- 光子晶体
- 透光石
- 磁力
- tda2003
- 故障指示器
- 2-(吡啶-2-基氨基)乙醇
- 基于10kV配电网地电位搭火线夹设计与节能性
- 建筑电气工程DQ2.15等电位联结施工隐蔽验收记录
- 电气等电位联结工程隐蔽验收记录
- RuO2/TiO2电极在海水电解防污中电化学行为
- 什么是汇流铜排\什么是等电位箱它们的应用及解决方案
- 电极材料发展趋势及应用前景
- 地电位更换110kV线路小间距双回路耐张塔绝缘子串
- Al2O3弥散强化铜电极点焊镀铝钢板行为
- 地下配电室重复接地、防雷接地、等电位接地
- CrZrCu电阻点焊电极焊接镀锌钢板失效原因
- 氟离子电极和氟离子电极价格
- 500kV输电线路ZVJ型杆塔进入等电位方式
- 不等电极距情况下高密度电阻率法的反演结果分析
- 低驱动电位AlGa合金牺牲阳极及其活化机制
- 双电极焊条两芯间距和焊接电流对单弧焊工艺的影响
- 500kV变电站等电位连接铜缆方式研究

