铵根离子
铵根正离子(Ammonium;化学式:NH4)是由氨分子衍生出的正离子。氨分子与一个氢离子配位结合就形成铵离子(氨提供孤对电子)。由于化学性质类似于金属离子,故命名为"铵"。
铵根离子基本信息
| 中文名称 | 铵根离子 | 外文名称 | Ammoniumion |
|---|---|---|---|
| 汉语拼音 | ǎn gēn lí zǐ | 化合价 | 正一价 |
由于铵盐中含氮,铵盐可用作氮肥,称为铵态氮肥。此类肥料不宜与碱性肥料混用,否则铵离子会被反应掉从而肥效降低。
常见的铵态氮肥有硫铵、碳铵、硝铵。
铵根离子造价信息
要区别碳铵于其他的铵盐,可以通过加热的方式。
NH4HCO3=△=NH3↑+H2O+CO2↑
但请注意:这个方法最好不要用于鉴别硝酸铵,因为硝酸铵遇高温容易发生爆炸。
酸性环境下,溶解在水中的氨分子以一水合氨或铵根离子的形式存在。浓氨水容易大量挥发出氨气。液氨自耦电离能产生铵离子和氨基离子。
铵根离子常见问题
-
它是分子,可形成TBAB+阳离子四丁基溴化铵;其它名称:其它名称:TBAB、TBA溴化物、四正丁基氨基溴化物、溴化四丁铵, N,N,N-三丁基-1-丁铵溴化物
-
硝酸根离子如果在酸性环境中,就不能和具有还原性的离子,比如亚铁离子, 碘离子,硫离子等离子共存。其他情况下都能共存。
-
氯化铵溶液呈酸性铵根水解NH4++H2O可逆号NH3.H2O+H+
铵根离子还可以和阴离子结合形成盐,大部分铵盐都可溶(如硅酸铵溶于水会双水解)。
常见的铵盐有:
氯化铵 硝酸铵 碳酸氢铵 一般的铵盐命名为某化铵或某酸铵,如氯化铵、醋酸铵等。
季胺盐,即NH4的4个氢均被烃基取代的产物与阴离子形成的盐。
铵根离子文献

 硫氰酸铵容量法测定管道压浆料(压浆剂)的氯离子含量
硫氰酸铵容量法测定管道压浆料(压浆剂)的氯离子含量
简单介绍了管道压浆料、压浆剂的组成和施工使用方法,基于笔者的工作经验和管道压浆料、压浆剂组分的复杂性,确定硫氰酸铵容量法结合电位滴定法判定滴定终点为测定混凝土管道压浆料(压浆剂)的氯离子含量的适宜方法。
化学式:NH4
立体构型:正四面体型,与甲烷互为等电子体。
定义:是由氨分子衍生出的正价离子。氨分子得到一个质子就形成铵离子。由于化学性质类似于金属离子,故命名为“铵”,属于原子团。
铵根遇大量氢氧根(OH-)易生成氨气(NH3)和水:
铵盐一般为易溶于水的白色晶体,可用做肥料。
铵盐皆为晶体,易溶于水,常伴有吸热现象。在水溶液中水解一般呈弱酸性(除某些弱酸Ka值≤氨的Kb值的铵盐,例如醋酸铵、氰化铵等)。
加热则出NH3,是铵盐的重要检验方法之一。热分解情况与对应的酸有关。一般非氧化性酸的铵盐(如NH4Cl,NH4Br,(NH4)3PO4等)热分解产物为NH3与对应酸。氧化性酸的铵盐热分解比较复杂,产物有N2或其氧化物出现,如:
强酸铵盐与弱酸铵盐相比,弱酸铵盐的稳定性较差,如NH4HCO3,(NH4)2CO3等在常温条件下就缓慢分解成NH3、CO2和水蒸气而损失。
铵根鉴定方式
碱性溶液中的(奈斯勒试剂或称铵态氮试剂)是鉴定铵根离子的特效试剂。
在试液中加入少量氢氧化钾,然后煮沸,将沾有奈斯勒试剂的滤纸放在试管口检测逸出气体中是否有氨气。
如果没有干扰离子可以直接往试液中加入奈斯勒试剂检验。
奈氏试剂检验铵离子的主要反应式为:
2HgI42- NH4 4OH-=[Hg2NH2O]I(红) 7I- 3H2O
作用后产生黄色或棕色(高浓度时)沉淀。
制备方式
①制备四碘合汞(II)酸银(I):Ag2(HgI4),在45~50℃由黄色可逆地变为红色。
2AgNO3 K2(HgI4)=Ag2(HgI4)↓ 2KNO3
②制备四碘合汞(II)酸铜(I):Cu2(HgI4),在71℃由红色变为黑紫色。
2CuSO4 K2(HgI4) SO2 2H2O=Cu2(HgI4) K2SO4 2H2SO4
铵根铵盐的碱解
铵盐会和强碱溶液在加热条件下反应生成NH3,离子方程如下:
一般使用NH4Cl和NaOH:
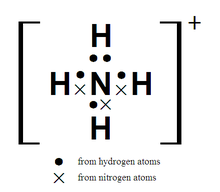
铵性质
由氨衍生的一种离子NH₄或基"―NH₄"。也叫"铵根",它是化 学中的一种阳性复根,用NH₄表示。它和一价金属离子相似。它的盐类称为铵盐。如化肥硫铵和碳酸铵的分子都含有铵。
铵离子的性质和钾离子相近,在溶液中呈+1价。铵盐都呈白色晶体,加碱研磨(相当于加热)能生成有刺激性气味的氨气(化学式:NH₃),铵盐受热会分解。
还原性
铵根离子有较强的还原性,其中的负三价的氮化合价上升的趋势较强,会被强氧化剂氧化成N2,氮氧化物甚至NO3。相关反应式:
与溴反应:3Br2+2NH4=3Br+N2↑+8H
与双氧水反应:3H2O2+2NH4=N2↑+2H+6H2O
与氯气反应:3Cl2+2NH4=3Br+N2↑+8H
与亚硝酸反应:5HNO2+NH4=6NO↑+4H2O+H
硝酸铵爆炸:NO3+NH4=(加热或撞击)=N2O↑+2H2O
与浓硝酸反应:7NO3+6H+NH4=8NO2↑+5H2O
与稀硝酸反应:5NO3+3NH4+2H=8NO↑+7H2O
与氧气反应:第一步5O2+4NH4=(加热,Pt催化剂)=4NO↑+6H2O+4H
第二步:4NO+3O2+2H2O=4NO3+4H
总反应:2O2+NH4=(加热,Pt催化剂)=NO3+H2O+2H
与次氯酸钠反应:4ClO+NH4=4Cl+NO3+H2O+2H
与重铬酸反应:(1)稀:Cr2O7+2NH4+6H=2Cr+N2↑+7H2O
(2)中:7Cr2O7+6NH4+50H=14Cr+6NO2↑+37H2O
(3)浓:4Cr2O7+3NH4+26H=8Cr+3NO3+19H2O
与高锰酸反应:(1)稀:8MnO4+5NH4+14H=8Mn+5NO3+17H2O
(2)浓:8MnO4+3NH4+2H=8MnO2↓+3NO3+7H2O
- 相关百科
- 相关知识
- 相关专栏
- 绿萍
- 湖南赤马湖滑雪场
- temed
- 万能办公台2Beta
- 辽粳28
- 会客椅
- 卡灵顿
- 侯氏制碱法
- 脲铵氮肥
- 办公椅座背耐久性试验机
- 聚羧酸母液
- SDS聚丙烯酰胺凝胶电泳
- 第六届工艺品展
- CNIBEE2012广州国际生物质能源技术及设备展
- 烟气脱硫方法
- 甲基咪唑
- 磷铵技术改造五大磷肥工程的建议
- 防盗门装进门洞打六根膨胀螺丝固定
- 智能点型离子感烟探测器和普通感烟探测器有什么区别
- 影响混凝土建筑物氯离子电通量因素的试验与分析
- 怎样正确连接三相电动机接线盒内已混乱的六根引出线
- 功率参数对超音速等离子制备高铝铜合金涂层组织影响
- 改性聚磷酸铵在室内水性超薄型钢结构防火涂料中应用
- 公路工程招投标中围标串标行为成因及根治措施分析
- 机械球磨与放电等离子体烧结制备碳纳米管/铜复合材料
- 兰州重离子加速器冷却储存环中束流位置测量系统研制
- 小水电代燃料工程建设桑植生态环境根本好转
- 既有铁路电气化改造中接触网桥钢柱生根组立方案
- 挤压混凝土边墙施工技术在中葛根水库面板堆石坝应用
- 氯离子侵蚀不同荷载下的钢筋混凝土梁正截面承载能力研究
- X射线K边减影成像研究铜离子在聚合物材料上的吸附
- 330MW热电联产机组汽包锅炉等离子点火系统技术改造
