05第二类医疗器械经营场所地理位置图、平面图
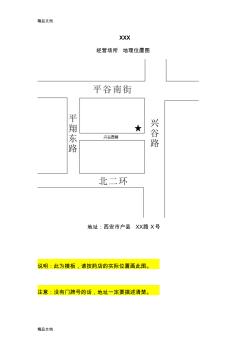
XXX 经营场所 地理位置图 地址:西安市户县 XX路 X号 说明:此为模板,请按药店的实际位置画此图。 注意:没有门牌号的话,地址一定要描述清楚。 西安中药集团户县公司庞光药店中西药门市部 经营场所 平面图 单位: cm 建筑面积: 44㎡ 实际使用面积: 40㎡ 说明:此为模板,请按药店实际画此图 注意事项: 1、要标示出正北方在哪个方向; 2、要标示出平面尺寸; 3、标注出医疗器械在店内的摆放位置; 4、写出建筑面积和实际使用面积。 也可以你简单手画一下,我来帮你在电脑上画。 租赁合同复印件 房产证复印件
最新05第二类医疗器械经营场所地理位置图、平面图资料
精品文档 精品文档 xxx 经营场所地理位置图 地址:西安市户县xx路x号 说明:此为模板,请按药店的实际位置画此图。 注意:没有门牌号的话,地址一定要描述清楚。 精品文档 精品文档 西安中药集团户县公司庞光药店中西药门市部 经营场所平面图 单位:cm 建筑面积:44㎡ 实际使用面积:40㎡ 说明:此为模板,请按药店实际画此图 精品文档 精品文档 注意事项:1、要标示出正北方在哪个方向;2、要标示出平面尺寸; 3、 4、标注出医疗器械在店内的摆放位置;4、写出建筑面积和实际使用面积。 也可以你简单手画一下,我来帮你在电脑上画。 租赁合同复印件 房产证复印件
编辑推荐下载
6、经营场所与库房地理位置图、平面图
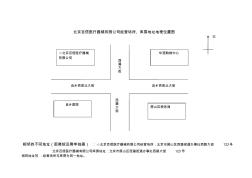
北京百信医疗器械有限公司经营场所、库房地址地理位置图 相邻的不同地址(距离较远需单独画):☆北京百信医疗器械有限公司经营场所:北京市房山区西潞街道办事处西路大街122号 北京百信医疗器械有限公司库房地址:北京市房山区西潞街道办事处西路大街123号 相同地址写:经营场所与库房为同一地址。 ☆北京百信医疗器械 有限公司 华冠购物中心 良乡医院 房山区税务局 良乡拱辰北大街良乡拱辰北大街 西 潞 大 街 西 潞 大 街 北 北京百信医疗器械有限公司经营场所、库房地址地理位置图 相邻的不同地址(距离较远需单独画):☆北京百信医疗器械有限公司经营场所:北京市房山区西潞街道办事处西路大街122号 北京百信医疗器械有限公司库房地址:北京市房山区西潞街道办事处西路大街123号 相同地址写:经营场所与库房为同一地址。 家乐福超市良乡店 良乡医院 国泰百货上场 电业大厦 北 拱 辰 大 街
经营场所库房地址的地理位置图平面图房屋产权证明文或者租赁协议
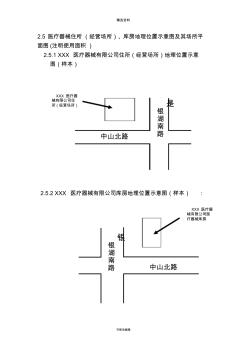
精选资料 可修改编辑 2.5医疗器械住所(经营场所)、库房地理位置示意图及其场所平 面图(注明使用面积) 2.5.1xxx医疗器械有限公司住所(经营场所)地理位置示意 图(样本) 2.5.2xxx医疗器械有限公司库房地理位置示意图(样本): xxx医疗器 械有限公司住 所(经营场所) 银 银 湖 南 路中山北路 是 银 湖 南 路中山北路 xxx医疗器 械有限公司医 疗器械库房 精选资料 可修改编辑 2.5.3xxx医疗器械有限公司住所(经营场所)平面图(样本) 2.5.4xxx医疗器械有限公司库房平面图(样本) 经理室 财 务 部 质 管 部 展 品 室 业务部 售后服务部 使用面积:长26米,宽8米,共208平方米。 发 货 区 合格区 合格区 退 货 区 待 验 区 不合格区 仓库使用面积:长11米,宽8米,共88平方米。 精选资料 可修改编
第二类医疗器械经营场所地理位置图、平面图资料热门文档

河北省第二类医疗器械优先审批程序程序(试行)
河北省第二类医疗器械优先审批程序(试行) 第一条为保障河北省医疗器械临床使用需求,满足公众用 械需要,推动我省医疗器械产业健康发展,根据《医疗器械监督 管理条例》、《医疗器械注册管理办法》、《体外诊断试剂注册 管理办法》、《国务院关于改革药品医疗器械审评审批制度的意 见》和《总局关于发布医疗器械优先审批程序的公告》等有关规 定,制定本程序。 第二条河北省食品药品监督管理局(以下简称省局)对符 合下列条件之一的本省辖区内第二类医疗器械首次注册的申请 实施优先审批: (一)诊断或治疗罕见病,且具有明显临床优势的医疗器械; (二)诊断或治疗老年人特有和多发疾病,且目前尚无有效 诊断或治疗手段的医疗器械; (三)专用于儿童,且具有明显临床优势; (四)列入国家、河北省科技重大专项或国家、河北省重点 研发计划的医疗器械; (五)符合京津冀协同发展政策要求,由京津转移到河北的 医
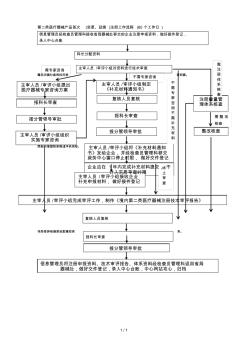
第二类医疗器械产品首次(变更、延续)注册工作流程(60个
1/1 不需专家咨询 需整改 核查 第二类医疗器械产品首次(变更、延续)注册工作流程(60个工作日) 信息管理员经检查员管理科接收省局器械处移交的企业注册申报资料,做好接件登记, 录入中心台账 科长分配资料 矚慫润厲钐瘗睞枥庑赖賃軔朧。 聞創沟燴鐺險爱氇谴净祸測樅。 残骛楼諍锩瀨濟溆塹籟婭骒東。 主审人员/审评小组对资料进行技术审查 复核人员复核 报科长审查 主审人员/审评小组制定 《补充材料通知书》 主审人员/审评小组将《补充材料通知 书》发给企业,并经检查员管理科移交 政务中心窗口停止时限,做好交件登记 企业应在1年内完成补充材料提交,不 计入实质审查时限 报分管领导审批 主审人员/审评小组完成审评工作,制作《境内第二类医疗器械注册技术审评报告》 主审人员/审评小组提出 医疗器械专家咨询方案 复核人员复核 报科长审查 报分管领导审批 主审人员/审评
第二类医疗器械经营场所地理位置图、平面图资料精华文档

境内第二类、第三类医疗器械重新注册申请材料要求
附件5: 境内第二类、第三类医疗器械重新注册申请材料要求 (一)境内医疗器械注册申请表; (二)医疗器械生产企业资格证明: 包括生产企业许可证、营业执照副本,并且所申请产品应当在生产企业许可证核定的生 产范围之内; (三)原医疗器械注册证书: 属于本办法第五章第三十三条情形的,提交原医疗器械注册证书复印件。属于本办法第 五章第三十四条、第三十五条情形的,应当提交原医疗器械注册证书原件; (四)医疗器械检测机构出具的产品注册检测报告: 需要进行临床试验的医疗器械,应当提交临床试验开始前半年内由医疗器械检测机构出 具的检测报告。不需进行临床试验的医疗器械,应当提交注册受理前1年内由医疗器械检测 机构出具的检测报告。 执行本办法第十一条、第十二条、第十三条、第十四条的规定的,应当提供相应的说明 文件; (五)适用的产品标准及说明: 采用国家标准、行业标准作为产品的适用标准
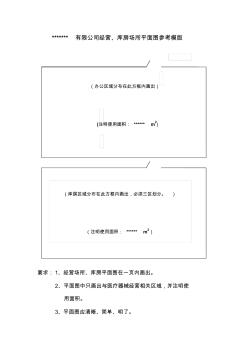
地理位置图、平面图 (2)
(库房区域分布在此方框内画出,必须三区划分。) (注明使用面积:******m2) *******有限公司经营、库房场所平面图参考模版 要求:1、经营场所、库房平面图在一页内画出。 2、平面图中只画出与医疗器械经营相关区域,并注明使 用面积。 3、平面图应清晰、简单、明了。 (办公区域分布在此方框内画出) (注明使用面积:******m2) *******有限公司注册地址地理位置图

核发第二类、第三类医疗器械生产企业许可证
核发第二类、第三类医疗器械生产企业许可证 项目名称:核发第二类、第三类医疗器械生产企业许可证 ①核发第二类、第三类医疗器械生产企业许可证 审批依据:《医疗器械监督管理条例》(国务院令第276号)、《医疗器械生产监督管理办 法》(国家食品药品监督管理局第12号令) 申报条件: 1、企业的生产、质量和技术负责人应当具有与所生产医疗器械相适应的专业能力,并 掌握国家有关医疗器械监督管理的法律、法规和规章以及相关产品质量、技术的规定。质量 负责人不得同时兼任生产负责人; 2、企业内初级以上职称或者中专以上学历的技术人员占职工总数的比例应当与所生产 产品的要求相适应; 3、企业应当具有与所生产产品及生产规模相适应的生产设备,生产、仓储场地和环境。 企业生产对环境和设备等有特殊要求的医疗器械的,应当符合国家标准、行业标准和国家有 关规定; 4、企业应当设立质量检验机构,并具备与所

第二类、第三类医疗器械生产企业需要满足什么条件
第二类、第三类医疗器械生产企业需要满足什么条件 (一)企业的生产、质量和技术负责人应当具有与所生产医疗器 械相适应的专业能力,并掌握(奥咨达医疗器械咨询) 国家有关医疗器械监督管理的法律、法规和规章以及相关产品质 量、技术的规定。质量负责人不得 同时兼任生产负责人; (二)企业内初级以上职称或者中专以上学历的技术人员占职工 总数的比例应当与所生产产品 的要求相适应;(只专注于医疗器械领域) (三)企业应当具有与所生产产品及生产规模相适应的生产设 备,生产、仓储场地和环境。企 业生产对环境和设备等有特殊要求的医疗器械的,应当符合国家 标准、行业标准和国家有关规定; (四)企业应当设立质量检验机构,并具备与所生产品种和生产 规模相适应的质量检验能力; (五)企业应当保存与医疗器械生产和经营有关的法律、法规、 规章和有关技术标准。 开办第三类医疗器械生产企业,除应当符合以上要求外,还应当
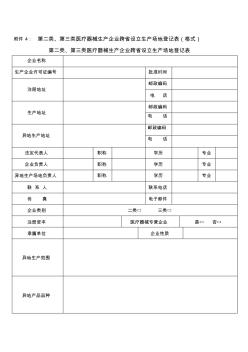
第二类、第三类医疗器械生产企业跨
附件4:第二类、第三类医疗器械生产企业跨省设立生产场地登记表(格式) 第二类、第三类医疗器械生产企业跨省设立生产场地登记表 企业名称 生产企业许可证编号批准时间 注册地址 邮政编码 电话 生产地址 邮政编码 电话 异地生产地址 邮政编码 电话 法定代表人职称学历专业 企业负责人职称学历专业 异地生产场地负责人职称学历专业 联系人联系电话 传真电子邮件 企业类别二类□三类□ 注册资本医疗器械专营企业是□否□ 隶属单位企业性质 异地生产范围 异地产品品种 异地生产场地基本情况 职工总数技术人员数 异地生产场所 状况(m2) 建设总面积其中 生产面积净化面积检验面积仓储面积 检验机构状况总人数技术人员数 企业意见 法定代表人签字: 年月日 企业盖章: 年月日 审核意见 签字:年月日 注册地省级(食 品)药品监督管
第二类医疗器械经营场所地理位置图、平面图资料最新文档
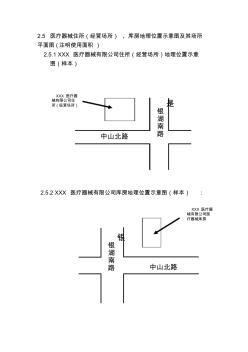
完整word版,经营场所、库房地址的地理位置图、平面图、房屋产权证明文件或者租赁协议
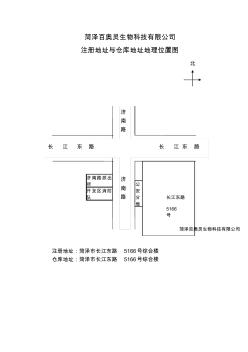
2.5医疗器械住所(经营场所)、库房地理位置示意图及其场所 平面图(注明使用面积) 2.5.1xxx医疗器械有限公司住所(经营场所)地理位置示意 图(样本) 2.5.2xxx医疗器械有限公司库房地理位置示意图(样本): xxx医疗器 械有限公司住 所(经营场所) 银 银 湖 南 路中山北路 是 银 湖 南 路中山北路 xxx医疗器 械有限公司医 疗器械库房 2.5.3xxx医疗器械有限公司住所(经营场所)平面图(样本) 2.5.4xxx医疗器械有限公司库房平面图(样本) 经理室 财 务 部 质 管 部 展 品 室 业务部 售后服务部 使用面积:长26米,宽8米,共208平方米。 发 货 区 合格区 合格区 退 货 区 待 验 区 不合格区 仓库使用面积:长11米,宽8米,共88平方米。
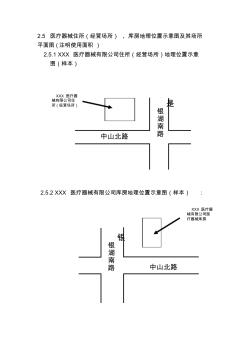
经营场所、库房地址的地理位置图、平面图、房屋产权证明文件或者租赁协议
2.5医疗器械住所(经营场所)、库房地理位置示意图及其场所 平面图(注明使用面积) 2.5.1xxx医疗器械有限公司住所(经营场所)地理位置示意 图(样本) 2.5.2xxx医疗器械有限公司库房地理位置示意图(样本): xxx医疗器 械有限公司住 所(经营场所) 银 银 湖 南 路中山北路 是 银 湖 南 路中山北路 xxx医疗器 械有限公司医 疗器械库房 2.5.3xxx医疗器械有限公司住所(经营场所)平面图(样本) 2.5.4xxx医疗器械有限公司库房平面图(样本) 经理室 财 务 部 质 管 部 展 品 室 业务部 售后服务部 使用面积:长26米,宽8米,共208平方米。 发 货 区 合格区 合格区 退 货 区 待 验 区 不合格区 仓库使用面积:长11米,宽8米,共88平方米。
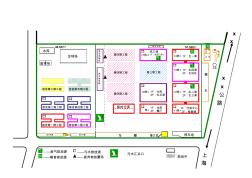
厂区地理位置与平面图
压空 房 油库 临时仓库 废 弃 物 仓 库 临时仓库 危 险 品 仓 库 x x 公 路 上 海 水塔 配 所 电 车 棚 第四期工程 第四期工程 第四期工程 第三期工程 栋> 1f:仓库 2f:餐厅 1f:行政中心 2f:检查课 1f:仓库 2f:生五课 1f:生二课 2f:生三课 1f:生四课 2f:生技处 1f:生一课(1f:成型工程) 机工课 81,520㎡40,937㎡ 水库 蓝球场 足球场 宿舍第六期工程宿舍第五期工程 宿舍第三期工程宿舍第四期工程 宿舍第一期工程宿舍第二期工程 自行车棚自行车棚警卫室 规划中 ——污水排放源 ——废弃物放置场 污水汇总口 x x 车棚停车场警卫室 ——废气排放源 ——噪音排放源

第一类医疗器械备案资料
第一类医疗器械备案资料 品名:******* *******有限公司 目录 一、第一类医疗器械备案表⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯ 二、产品风险分析报告⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯ 三、产品技术要求⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯ 四、产品检验报告⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯ 五、临床评价资料⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯ 六、产品使用说明书及最小销售标签样稿⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯ 七、生产制造信息⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯ 八、证明性文件⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯ 九、符合性声明⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯ 十、授权委托书⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯

经营场所平面图(20200706211321)
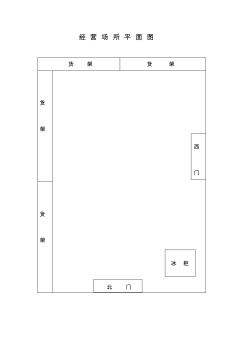
乾县北什字 中西药店经营场所平面图 保健品专柜otc货架 用 药 咨 询 台 干湿温度计空 调 器械柜台 otc 货架 otc 货架 otc 货架 otc 货架 中 药 柜 rx 柜 台 rx 柜 台 电脑 rx 柜 台 易串味药品柜台 不合格区 退货区待验区 冰箱饮水机 条 椅 条 椅 6.15m 10 .5 m 北 东西 南 东 南 门 中 门 北 门
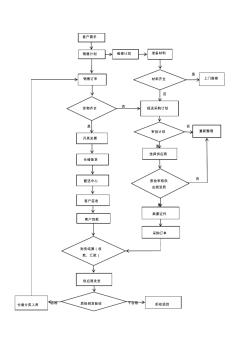
医疗器械公司流程图-精选
是 否 否 是否 是 否 是 合格不合格 客户需求 销售计划维修计划准备材料 材料齐全上门维修 报送采购计划 销售订单 货物齐全 开具发票 仓储备货 配送中心 客户签收 审批计划重新整理 选择供应商 质检审核供 应商资质 索要证件 采购订单 客户回款 财务结算(收 款、汇款) 供应商发货 质检到货验收拒收退回仓储分类入库

第一类医疗器械备案资料要求及说明
附件8 第一类医疗器械备案资料要求及说明 一、申请表 应按照要求完整填写注册申请表。 二、产品风险分析资料 对产品进行安全风险管理相关情况概述 三、产品技术要求 四、产品检验报告 产品全性能自检报告或委托检验报告。 五、临床评价资料 (一)产品预期用途的描述; (二)与产品使用有关的临床风险分析; (三)已上市同类产品临床使用情况的比对说明; (四)其他证明产品安全性、有效性的研究资料或文献资料。 六、生产制造信息 对生产过程相关情况的概述。 七、产品说明书及最小销售单元的包装、标签设计样稿 八、证明性文件 (一)境内备案人提供:企业法人营业执照副本。 (二)境外备案人提供: 1.境外备案人所在国家(地区)医疗器械主管部门出具的 允许产品上市销售的证明文件; 2.境外备案人在中国境内指定代理人的委托书、代理人承 诺书及营业执照副本或者机构登记证明复印件。 九、符合性声明 (一)
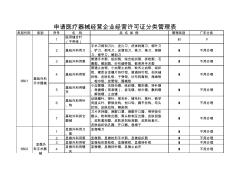
医疗器械分类目录经营分类表
类别代码类别序号名称品名举例管理类别广东分类 1医用缝合针 (不带线) ⅱf 2基础外科用刀 手术刀柄和刀片、皮片刀、疣体剥离刀、柳叶刀 、铲刀、剃毛刀、皮屑刮刀、挑刀、锋刀、修脚 刀、修甲刀、解剖刀 ⅰ不用办理 3基础外科用剪普通手术剪、组织剪、综合组织剪、拆线剪、石 膏剪、解剖剪、纱布绷带剪、教育用手术剪 ⅰ不用办理 4基础外科用钳 普通止血钳、小血管止血钳、蚊式止血钳、组织 钳、硬质合金镶片持针钳、普通持针钳、创夹缝 拆钳、皮肤轧钳、子弹钳、纱布剥离钳、海绵钳 、帕巾钳、皮管钳、器械钳 ⅰ不用办理 5基础外科用镊 夹 小血管镊、无损伤镊、组织镊、整形镊、持针镊 、保健镊(简易镊)、拔毛镊、帕巾镊、敷料镊 、解剖镊、止血镊 ⅰ不用办理 6基础外科用针 、钩 动脉瘤针、探针、推毛针、植毛针、挑针、教学 用直尖针、静脉拉钩、创口钩、扁平拉钩、双
第二类医疗器械经营场所地理位置图、平面图资料相关
文辑推荐
知识推荐
百科推荐

职位:电气项目管理工程师
擅长专业:土建 安装 装饰 市政 园林