新版GMP颁布后药厂新建、改造设计审核
2011年2月12日《药品生产质量管理规范(2010年修订)》予以发布,自2011年3月1日起施行。新版药品GMP吸收国际先进经验,结合中国国情,按照"软件硬件并重"的原则,强调指导性和可操作性,达到了与世界卫生组织药品GMP的一致性。新版药品GMP的实施后,凡新建药品生产企业、药品生产企业新建(改、扩建)车间均应符合新版药品GMP的要20
编辑推荐下载

加固技术在某药厂GMP改造工程中的应用
结合工程实例,详细介绍了钢结构在钢筋混凝土结构加固改造工程中的推广应用。

药厂GMP洁净空调系统节能分析
药厂gmp洁净空调系统节能分析——对gmp洁净空调系统一次回风方式的两种设置方法在耗能方面进行比较,双表冷一次回风系统比单表冷一次回风系统节能30%,对全厂节能的贡献率约为10%。
GMP颁布后药厂新建、改造设计审核热门文档
FOPLC在制药厂GMP工程中的应用
《药品生产质量管理规范》,英文称为goodmanufacturingpractice,简称gmp。它是为保证药品生产质量需要而产生的,是药品生产企业进行药品生产质量管理必须遵守的基本准则,是当今国际社会通行的药品生产必须实施的一种制度,是把药品生产全过程中发生的差错、混药及各种污染的可能性降至最低程度的必要条件和最可靠的办法。

新版GMP要求下制药厂洁净空调使用与设计分析
主要就新版gmp的要求分析了制药厂净化空调系统在设计使用时碰到的常见问题和解决问题的方法,以节省投资和运行费用,满足gmp对净化工程的要求。
水磨石表面改性技术在药厂GMP改造中的应用
介绍了一种全新的水磨石地面的表面改性技术,主要是利用化学反应与纳米渗透对制药车间水磨石等地面材料表面进行改性处理,形成一个符合gmp认证标准的表面层。该技术对于降低制药企业改造成本具有积极的意义。

制药厂与GMP制药企业洁净厂房百级洁净区作法探讨
制药厂与gmp制药企业洁净厂房百级洁净区作法探讨——药品生产厂房洁净车间内,经常会有局部百级区,或要求某一个房间或几个房间为百级,或要求某个房间内部分区域为百级,这些百级区面积一般都不大,从几十平方米到几平方米甚至零点几平方米不等,通常为一个洁净区内...

药厂GMP工程洁净空调施工调试检测技术
介绍gmp工程洁净空调系统的主要安装施工工艺及其技术措施,总结洁净空调系统的质量要求和检测方法,以及在工程实施中的具体做法。
GMP颁布后药厂新建、改造设计审核精华文档

昆明某制药厂药品gmp洁净厂房改造工程施工组织设计
昆明xx制药厂 药品gmp洁净厂房改造工程 施 工 组 织 设 计 1、综述 1.1概述 本工程地处昆明xx西路与xxx路交叉路口西南角,xx立交桥旁,属老厂房 改造。昆明xx制药厂gmp洁净厂房改造工程含洁净区彩钢隔断及净化空调工 程与公用工程——公用工程内容包括给排水、电气(动力系统、照明、弱 电)、工艺管道(压缩空气、真空管道)、厂区管网及消防系统等安装工程。 建筑规模共约2124m2。其中,洁净面积约441m2,主要集中在二层(有液体口 服制剂及胶囊、片剂生产线;三层“卫生学检验”只约15m 2 洁净区)。本工 程由云南省第二安装工程公司(总承包一级资质企业)抬头联合兰德设计所 (医学乙级)向昆明xx制药厂进行设计及施工总承包(内容含“gmp洁净厂 房改造工程”及2736m2的“配套钢结构工程”)——以顾客满意为宗旨,在 保证质量、保证

2019年制药厂药品gmp洁净厂房改造工程施工组织设计
铫胧 昆明xx制药厂铫胧 药品gmp洁净厂房改造 工程铫胧 1.1概述铫胧 本工程地处昆明xx西路与xxx路交叉路口西南角,xx立交桥旁,属老厂房改造。昆明xx 制药厂gmp洁净厂房改造工程含洁净区彩钢隔断及净化空调工程与公用工程——公用工 程内容包括给排水、电气(动力系统、照明、弱电)、工艺管道(压缩空气、真空管 道)、厂区管网及消防系统等安装工程。建筑规模共约2124m2。其中,洁净面积约 441m2,主要集中在二层(有液体口服制剂及胶囊、片剂生产线;三层“卫生学检验” 只约15m2洁净区)。本工程由云南省第二安装工程公司(总承包一级资质企业)抬头 联合兰德设计所(医学

医药工业厂房实施GMP改造的几点体会
在新修订的《药品管理法》已开始实施和我国成功加入世贸组织之既,国家药品监督管理局正式作出全面加快监督实施gmp工作进程的决定:2004年6月30日前、全国所有药品制剂和原料药生产必须符合gmp要求并取得gmp证书。截止2001年10月底,全国约有4800家制药企业需认证,而只有900家企业获gmp证书,仅占现有企业数量的19%,特别是95年前建成的老企业总体布局,工艺布局,不尽合理,厂房设备比较陈旧,自动化程度不高。因此实施gmp改造是很多企业面临求生存、谋发展的必由之路。现就我厂gmp改造项目工作情况浅谈几点体会。

方案样本宏达制药厂GMP厂房改造工程施工组织设计
昆明宏达制药厂gm洁净厂房改造工程投标文件施工组织设计 投标单位:云南省第二安装工程公司 昆明宏达制药厂 药品gmp洁净厂房改造工程 施 工 组 织 设 计 云南省第二安装工程公司 二00三年七月十六日 昆明宏达制药厂gm洁净厂房改造工程投标文件施工组织设计 投标单位:云南省第二安装工程公司 审批: 审核: 编制: 昆明宏达制药厂gm洁净厂房改造工程投标文件施工组织设计 投标单位:云南省第二安装工程公司 目录 1、综述 2、施工管理 3、确保gmp达标的保证措施 4、工期、进度计划 5、劳动力计划 6、暖通净化空调工程施工方案 6.1、净化工程主要检测仪表及施工机械 6.2、净化装修工程施工方案 6.3、净化空调工程施工方案 6.4、洁净区照明安装工程施工方案 7、公用工程施工方案 7.1、给排水及工艺管道

2010版药品GMP《实验室控制系统GMP实施指南》真正word版
实验室控制系统gmp实施指南 1前言 作为质量管理体系的一部分,质量控制实验室管理是确保所生产的药品适用于预定的用途, 符合药品标准和规定的要求的重要因素之一。 为了帮助制药企业中的实验室更好地满足gmp的要求,本指南主要参照国内外相关法规和 标准及指南对于实验室管理的阐述和要求,描述一个全面的实验室管理体系,以起到一定的指 导作用。 本指南的内容不具有法律约束性,超出现行gmp规定的内容是建议性和参考性的,而非强 制性要求,可以有选择地使用。 企业在运用本指南过程中,涉及到剂型特点或相关公用系统的内容时,还应参考其它配套 指南(见下表),并结合本企业的实际情况和现行法规要求开展相关工作。 表1-1指南逻辑关系图 质量管理 体系 设施设备水系统空调系统物料质量控制其它 口服固体 对于系统指南和制剂指南共有的内容,系统指南强调系统的通用程序的建立、 实施和管理过程;
GMP颁布后药厂新建、改造设计审核最新文档

GMP认证程序
38-13_药品生产质量管理规范认证 发布时间:2011-04-26 药品生产质量管理规范认证 许可项目名称: 编号:38-13 法定实施主体:北京市药品监督管理局 依据: 1、《中华人民共和国药品管理法》(中华人民共和国主席令第45号第九条) 2、《中华人民共和国药品管理法实施条例》(中华人民共和国国务院令第360号第五条至第七条) 3、《药品生产质量管理规范(1998年修订)》(国家药品监督管理局令第9号) 4.《药品生产质量管理规范(2010年修订)》(中华人民共和国卫生部令第79号) 5.《药品生产监督管理办法》(国家食品药品监督管理局令第14号第九条) 6.《药品生产质量管理规范认证管理办法》(国药监安[2005]437号第三条至第二十三条) 7.国家食品药品监督管理局关于印发《药品gmp认证检查评定标准》的通知(国食

XX制药厂GMP厂房改造工程施工组织设计含公用工程
药品gmp洁净厂房改造工程 施 工 组 织 设 计 审批: 审核: 编制: 目录 1、综述 1.1概述 本工程地处昆明人民西路与西二环路交叉路口西南角,西苑立交桥旁,属 老厂房改造。昆明宏达制药厂gmp洁净厂房改造工程含洁净区彩钢隔断及净 化空调工程与公用工程——公用工程内容包括给排水、电气(动力系统、照 明、弱电)、工艺管道(压缩空气、真空管道)、厂区管网及消防系统等安装 工程。建筑规模共约2124m2。其中,洁净面积约441m2,主要集中在二层 (有液体口服制剂及胶囊、片剂生产线;三层“卫生学检验”只约15m2洁 净区)。本工程由云南省第二安装工程公司(总承包一级资质企业)抬头联 合兰德设计所(医学乙级)向昆明宏达制药厂进行设计及施工总承包(内容 含“gmp洁净厂房改造工程”及2736m2的“配套钢结构工程”)——以顾 客满

某药业公司GMP改造工程质量计划
某药业公司gmp改造工程质量计划——该工程我方主要工作内容为制剂车间的净化空调、工艺设备、工艺管道、电气和净化区装修的安装。 本质量计划是向顾客提供本项目部履行合同的质量保证。 本质量计划也作为公司内部对该工程项目质量活动过程和结果进行...

新版GMP年度自检计划
湖南亚大制药有限公司 2014年度自检计划 1.自检目的:通过自检确保公司持续、有效地执行gmp规范,通过 定期地gmp自检确认公司执行gmp的符合性,找出改进机会,实 现持续改进。 2.自检依据:药品生产质量管理规范(2010修订版) 3.内容: 一、现场检查时间安排 现场检查时间安排于2014年9月-12月 二、参加自检人员 公司自检小组成员 三、自检首次会议 参加人员为公司自检小组成员,明确各成员的职责(质量管理 部负责人:负责自检工作的协调、管理工作,批准自检方案,和自检 报告。向公司管理层上报自检结果。gmp办主管:负责自检工作的 实施。各自检小组组长:提出自检小组名单,全面负责自检实施活动, 审核自检方案和自检报告。qa:负责编制自检计划并通知相关部门 和人员,组建自检小组,协调自检工作,准备自检文件,按照自检计 划实施自检,收集自检记

新版GMP实施过程中厂房改造的探讨
本文对新版gmp的实施过程中是否新建或改造厂房、项目实施的组织体系保证、厂房设计及工艺布局、项目设计环节客观科学的风险评估、项目实施过程中的质量控制、充分预估项目的资源以做好项目的进度管理等方面进行了阐述,以便在有限的时间内既按照工程要求完成厂房的新建或改造验收,又确保厂房符合预定用途及新版gmp的要求,为保证日后持续稳定地生产提供借鉴。
药厂GMP改造中有关传递窗的改造
药厂为达到gmp认证要求,为保证药品生产洁净区的洁净度符合国家标准,应对老式传递窗进行改造。方法:增加空气自净系统,双门互锁和声光提示,安装紫外灯,并随环境消毒。结论:有检测数据表明,改造后的传递窗内部洁净度达到100级,并对内部生产洁净区起到了很好的保护作用。

XX制药厂GMP车间改造项目——净化中央空调系统工程实例
结合xx制药厂gmp车间改造项目净化中央空调工程系统工程实例,介绍对本系统中送、回风系统、排风系统、除尘系统的设计思路。对此工程在应用过程中的优越性进行讨论,并分别分析此工程送、回风系统、排风系统送、除尘系统的特点,使项目既保证净化要求又节能。

XX制药厂GMP车间改造项目——净化中央空调系统工程实例
结合xx制药厂gmp车间改造项目净化中央空调工程系统工程实例,介绍对本系统中送、回风系统、排风系统、除尘系统的设计思路。对此工程在应用过程中的优越性进行讨论,并分别分析此工程送、回风系统、排风系统送、除尘系统的特点,使项目既保证净化要求又节能。
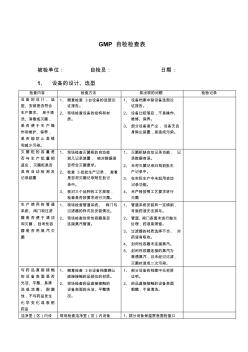
GMP培训资料--设备GMP自检检查表
gmp自检检查表 被检单位:自检员:日期: 1、设备的设计、选型 检查内容检查方法易出现的问题检验记录 设备的设计、选 型、安装是否符合 生产要求、易于清 洗、消毒或灭菌, 是否便于生产操 作和维护、保养, 是否能防止差错 和减少污染。 1、随意检查3台设备的选型论 证报告。 2、现场检查设备的结构和材 质。 1、设备档案中缺设备选型论 证报告。 2、设备比较落后,不易操作、 维修、保养。 3、部分设备易产尘,设备无自 身除尘装置,易造成污染。 灭菌柜的容量是 否与生产批量相 适应,灭菌柜是否 具有自动检测及 记录装置 1、现场检查灭菌柜的自动检 测几记录装置,核对数据是 否符合灭菌要求。 2、检查3批批生产记录,查看 是否将灭菌记录附在批记 录中。 3、核对三个品种的工艺规程, 检查是否按要求进行灭菌。 1、灭菌柜缺自动
规范铸造精品工程——记新百药业GMP工厂建设
规范铸造精品工程——记新百药业GMP工厂建设
GMP颁布后药厂新建、改造设计审核相关
文辑推荐
知识推荐
百科推荐

职位:城更规划师
擅长专业:土建 安装 装饰 市政 园林



