- 首页 >
- > 洁净厂房设计规范的内容

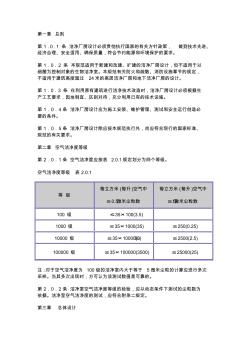
第一章 总则 第 1.0.1 条 洁净厂房设计必须贯彻执行国家的有关方针政策, 做到技术先进、 经济合理、安全适用、确保质量,符合节约能源和环境保护的要求。 第 1.0.2 条 本规范适用于新建和改建、扩建的洁净厂房设计,但不适用于以 细菌为控制对象的生物洁净室。本规范有关防火和疏散、消防设施章节的规定, 不适用于建筑高度超过 24米的高层洁净厂房和地下洁净厂房的设计。 第 1.0.3 条 在利用原有建筑进行洁净技术改造时,洁净厂房设计必须根据生 产工艺要求,因地制宜、区别对待,充分利用已有的技术设施。 第 1.0.4条 洁净厂房设计应为施工安装、维护管理、测试和安全运行创造必 要的条件。 第 1.0.5条 洁净厂房设计除应按本规范执行外,尚应符合现行的国家标准、 规范的有关要求。 第二章 空气洁净度等级 第 2.0.1条 空气洁净度应按表 2.0.1规定划分为四个等级。 空气洁净度等级


国家医药管理局 医药工业洁净厂房设计规范 主编部门:国家医药管理局上海医药设计院 批准部门:国家医药管理局 施行日期:1997年1月1日 1 编 制 说 明 为在我国医药行业深入实施GMP, 适应医药工业洁净厂房建设的需要, 国家 医药局推行GMP .GSP委员会设计规范专业组决定组织编写《医药工业洁净厂 房设计规范》。 本规范由上海医药设计院主编, 缪德华同志执笔, 武汉医药设计院、 重庆医药 设计院等单位参与。 在编写过程中广泛眚注医药行业内有关方面意见, 并先后数次 组织医药设计单位和大中型骨干企业的专家进行了认真的讲座修改, 由局推行GM P .GSP委员会寓言并原则通过。之后,局综合经济司(原局计划)就规范主要 内容向卫生部药政局、 药品监督办公室的领导、 专家征询了意见并得到了他们的理 解和支持。在此基础上,局GMP设计规范专业组对本规范作了修改定稿。 本规范编制工作结合国内
热门知识
洁净厂房设计规范的内容-
话题: 建筑设计amandadong
-
话题: 室内设计fangchaoqun
精华知识
洁净厂房设计规范的内容-
话题: 工程造价xuyuting01
最新知识
洁净厂房设计规范的内容-
话题: 工程造价angual_sun
-
话题: 建筑设计konglong1968
洁净厂房设计规范的内容知识来自于造价通云知平台上百万用户的经验与心得交流。 注册登录 造价通即可以了解到相关洁净厂房设计规范的内容最新的精华知识、热门知识、相关问答、行业资讯及精品资料下载。同时,造价通还为您提供材价查询、测算、询价、云造价等建设行业领域优质服务。手机版访问:洁净厂房设计规范的内容
- 洁净厂房设计规范的内容
- 洁净度等级标准有哪些
- 洁净厂房的车间板材
- 洁净厂房负荷如何计算
- 洁净车间设计与装修方案
- 洁净车间用什么材质的风管
- 洁净气体灭火器充装什么
- 洁净室工程怎样报价
- 洁净室里的新风量如何计算
- 洁净室一平方多少钱
- 基于压电堆驱动器的喷嘴挡板式气体控制阀
- 磷铵技术改造五大磷肥工程的建议
- 以大豆油多元醇制备的硬质聚氨酯泡沫塑料的性能
- 逆变TIG焊机接触引弧电路的设计(引弧电路)
- 应用模糊数学理论对公路工程建设项目方案的综合评价
- 可替代现有隔热保温材料的新型材料
- 以贯穿项目为核心载体的建筑工程技术专业素材库建设
- 多逆变器太阳能光伏并网发电系统的组群控制方法
- 影响萘高效减水剂与普通硅酸盐水泥适应性的关键因素
- 在全县非煤矿山和危化企业安全生产工作会议上的讲话
- 中国工程造价咨询业的发展趋势
- 支持并行工程和智能CAPP的制造资源建模技术
- 中共重庆市委重庆市人民政府关于建设平安重庆的决定
- 智能建筑工程报警与电视监控系统前端设备的安装施工
- 在“建筑节能与居住舒适”专题技术交流会议上的讲话
- 以MSP430FW427为核心的远程数字水表设计
- 园林绿化养护精细化管理对河源市园林景观的影响分析
- 洁净厂房设计与装修方案
- 洁净车间等级是多少
- 洁净车间设计与装修方案
- 洁净车间用什么材质的风管
- 洁净传递窗有什么功能
- 洁净度的具体标准
- 洁净度等级标准有哪些
- 洁净空调系统原理图计算
- 洁净棚为什么要加底板
- 洁净棚为什么用到FFU
- 洁净气体灭火器充装什么
- 洁净气体灭火器有哪些
- 洁净区人数如何计算
- 洁净室风机的材料什么好
- 洁净室工程公司施工步骤
- 洁净室工程施工有什么要求
- 洁净室工程验收规范有哪些
- 洁净室工程怎样报价
- 洁净室里的新风量如何计算
- 洁净室设计规范是什么
- 洁净室施工有哪些施工重点
- 洁净室一平方多少钱
- 洁具安装的规范要
- 洁具安装要什么辅料
- 洁具的安装高度的管径
- 洁具和卫浴有什么区别
- 洁具排水立管工程量计算
- 洁具四件套的水管怎么接
- 洁具四件套如何安装
- 洁具卫浴安装需要哪些工具



